
Разработка лекарств — сложный и дорогой процесс и количество неудач в клинических испытаниях, которые тестируют новые медикаменты на людях на предмет безопасности и эффективности остается высоким. Согласно текущим оценкам, только 13.8% всех тестируемых лекарств успешны и получают сертификацию у Администрации Продовольствия и Лекарств США (FDA). Также увеличивается количество проблем, связанных с тестированием на животных (вивисекция), поэтому постоянно ведется поиск средств замены животных на альтернативные методы для тестирования.
Для того, чтобы избежать этого бутылочного горлышка в разработке лекарств Дональд Ингбер (Donald Ingber) и его команда в институте Wyss Institute разработали первый в мире человеческий “орган-на-чипе” — модель легкого, которая повторяет физиологию и патофизиологию человеческого легкого с высокой степенью достоверности, сообщалось в журнале Science в 2010 году. Чипы-органы — это небольшие микрожидкостные устройства, сделанные из прозрачного гибкого полимера, внутри которых проходят два полых канала, разделённых пористой мембраной. Клетки, специфичные для конкретного органа, выращиваются с одной стороны такой мембраны одного из таких каналов, а васкулярно-эндотелиальные клетки, которые выращиваются с другой стороны — играют роль кровеносных сосудов. Каждый из каналов независимо заполняется клетками играющими роль переносчика (замена крови). Пористая мембрана позволяет двум отделениям сообщаться друг с другом, пропуская молекулы типа цитокинов, факторов роста и лекарств, а также продуктов реакции лекарств, которые создаются при специфичных для органа метаболических процессах.
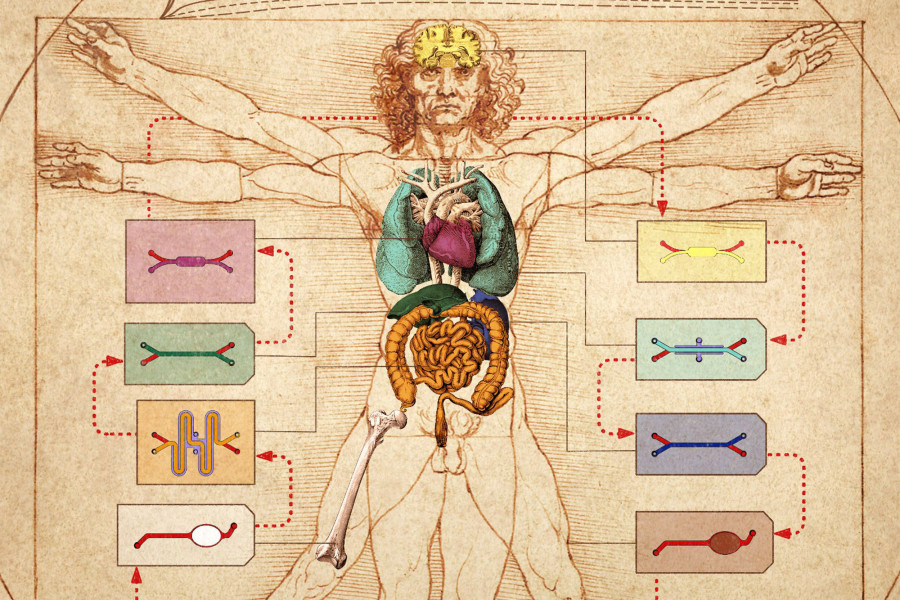
Один из примеров, где нужно использовать животных для доклинических испытаний — это определение фармакокинетики — определение поглощения, распределения, метаболизма и вывода препарата, которые вместе — определяют уровень лекарства в крови. Эти реакции организма — результат связной работы нескольких органов, связанных между собой сосудами, по которым течет кровь.
Поскольку чипы-органы содержат васкулярный канал, покрытый эндотелиальными клетками, Ингбер в 2011 году предположил, что может быть возможным создание человеческого “тела-на-чипе”, что позволит передавать жидкости между различными типами чипов-органов, чтобы повторить настоящее кровообращение и определять поведение лекарств с учетом всей связанной системы “органов”. Воодушевленное этой идеей и пониманием того, что текущие способы тестирования на животных не являются адекватным или быстрым способом разработки лекарств, особенно в условиях опасных ситуаций типа эпидемий или использования биологического оружия, Управление перспективных исследовательских проектов Министерства обороны США (DARPA) в 2012 году подало заявку на грант, в которой указала казалось бы невозможную цель — разработать 10 типов чипов-органов, которые бы воспроизводили бы сложную функциональность 10 разных человеческих органов, создать автоматизированный инструмент, при помощи которого эти органы можно было бы связать между собой и получить функциональную платформу “тело-на-чипе” и использовать компьютерное моделирование совместно с экспериментальными данными для точного определения поведения лекарств.


И вот были опубликованы две научных работы в журнале Nature Biomedical Engineering, которые заявляют о том, что вышеописанная цель достигнута полностью.
DARPA хорошо знакомы такие сверхсложные задачи, в которых довольно редко удается достичь полного успеха, но в процессе исследований в качестве сопутствующего результата довольно часто совершаются серьезные научные прорывы. “Мы были очень рады, что получили финансирование такого амбициозного проекта от DARPA, и ещё более горды теперь, когда нам удалось полностью достичь всех поставленных целей, что было бы невозможно без талантливых людей в нашей команде в Wyss Institute”, сказали Ингбер, который является директором-основателем Wyss Institute. Он руководил этим проектом вместе с Кевином Китом Паркером (Kevin Kit Parker), который является профессором биоинженерии и прикладной физики в SEAS.
В своей первой статье команда из института Wyss представила модульную платформу тело-на-чипе, которая возможным использование до 10 разных чипов-органов и последовательную передачу жидкостей между их васкулярными каналами, имитируя нормальный поток крови между разными органами в человеческом теле. Во второй статье команда использовала вычислительные методы чтобы интерполировать данные, полученные в результате эксперимента с использованием трех разных типов чипов-органов, в их реальное поведение в человеческом теле. Этот подход позволяет достоверно прогнозировать уровень веществ в крови с течением времени, а также специфичную для конкретных органов токсичность тех или иных медикаментов, что ранее тестировалось на реальных пациентах.
“Оба исследования показывают выдающийся результат исследователей из института Wyss, которые работали вместе с другими учеными и исследователями в других областях, таких, как инженерия живых тканей, микропроизводство, фармакология, физиология и вычислительная биоинженерия. Эти исследования позволяют перейти на качественно новый уровень в доклиническом тестировании медикаментов”, сказала Ракель Прантил-Баун (Rachelle Prantil-Baun), ведущий ученый института Wyss, которая координировала оба исследования.
Инструмент Interrogator позволил команде вырастить, питать и связать в единую мультиорганную систему многие живые человеческие ткани, а также ввести и исследовать среду переноса жидкостей в полностью управляемой конфигурации, одновременно с этим наблюдая за реакцией тканей при помощи встроенного микроскопа. В данном исследовании были связаны между собой такие чипы-органы, как пищеварительная система, печень, почка, сердце, легкое, кожа, гемо-энцефалический барьер и мозг, сообщающиеся между собой при помощи оптимизированного заменителя крови. Система жила в течении трех недель и позволила очень точно определить накопление и поведение химических веществ во всей системе.
Во втором исследовании команда использовала инструмент Interrogator для исследования трех различных конфигураций трех разных чипов-органов соединенных между собой при помощи артерио-венозной системы, которая позволила имитировать реальное поведение организма при обмене кровью и медикаментами между отдельными органами. Использовались такие органы, как кишечник, печень и почка. В чип-орган имитирующий кишечник был введен никотин, чтобы воспроизвести процесс перорального приема этого вещества, после чего он поступил в печень, где был метаболизирован и впоследствии выведен в почке. Исследование позволило точнее понять, как работает никотиновая жевательная резинка, которая используется не только как средство, помогающее бросить курить, но и является возможным лекарством при лечении нейродегенеративных и воспалительных процессов в желудке.
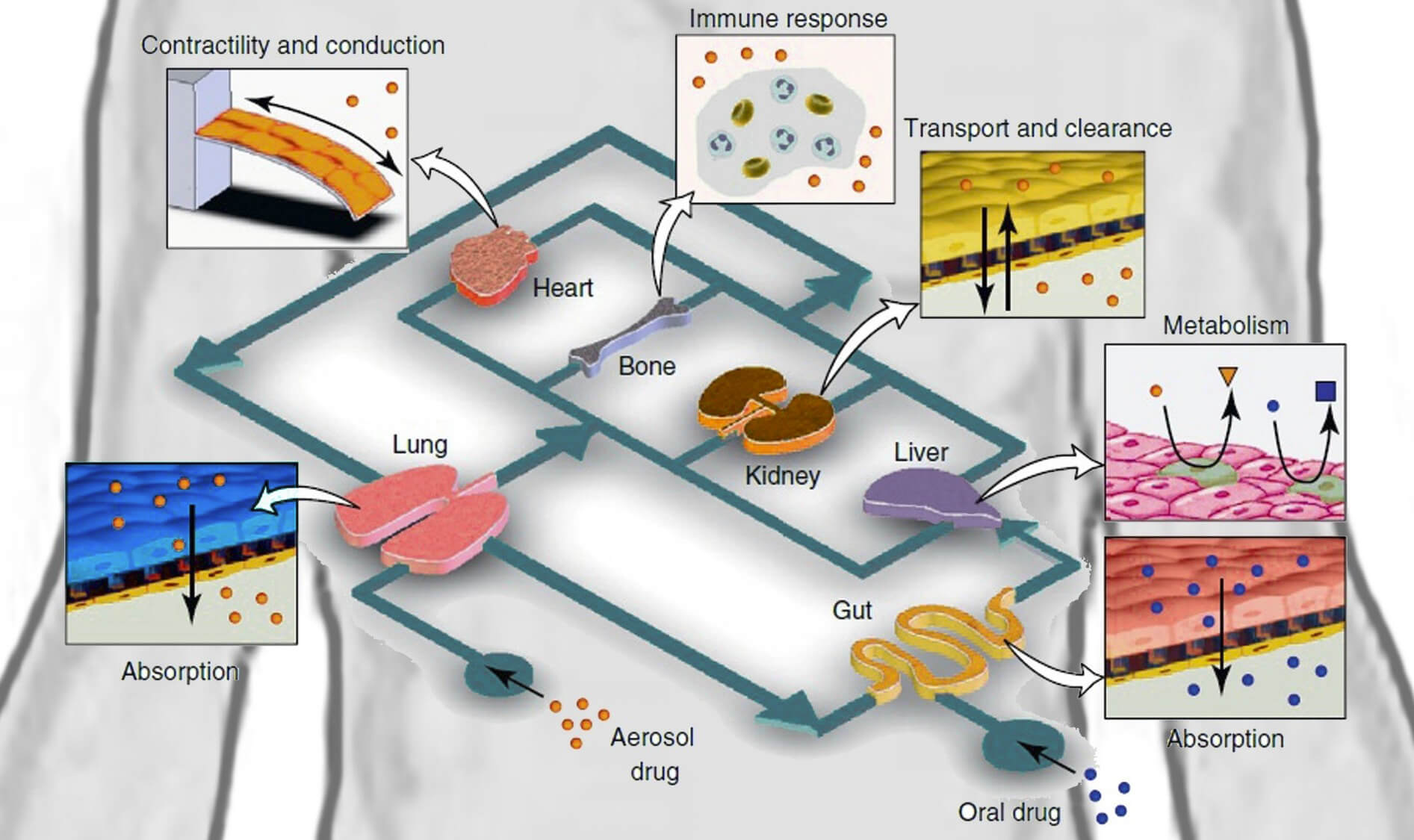
При помощи спектрального анализа команда смогла выяснить уровни никотина во всех чипах-органах и в артерио-венозной системе, после чего применить вычислительные методы для экстраполяции данных на человеческий организм. Данные полностью совпали с экспериментальными данными, полученными при клиническом исследовании на реальных пациентах.
Данные исследования и прорыв в этой области приближают людей к тому, что ранее считалось научной фантастикой — быстрое, высокоточное и гуманное, без использования животных, тестирование различных препаратов и лекарств.
Источник: save-animals.info

Отправить ответ
Для отправки комментария вам необходимо авторизоваться.